Properso Veesler

CRISTALLISATION ET MIGRATION EN SOLUTION
Stéphane VEESLER (E-mail)
Directeur de recherche au CNRS (section 05)Recherche au sein du département Sources et Sondes Ponctuelles
La cristallisation qui intervient à une interface solide liquide a pour but la purification mais aussi la mise en forme des particules produites. Ainsi dans le cas de la cristallisation industrielle on s'intéresse aux liens entre propriétés d'usage des matériaux, nucléation et croissance cristalline.
Nous développons une approche fondamentale de la cristallisation afin d'atteindre les objectifs définis au départ de l'étude avec le partenaire industriel ou académique. Nous étudions l'effet des paramètres de la cristallisation, sursaturation, température (à telecharger), additifs/impuretés, hydrodynamique, etc., sur le faciès, la morphologie, la distribution de taille des cristaux, les transitions de phases (polymorphisme et démixtion). (à telecharger-en Francais) : Polymorphisme dans les procédés de cristallisation en solution
(ou en Anglais) : Polymorphism in processes of crystallization in solution: a practical review
En biologie la connaissance structurale à l'échelle atomique est nécessaire pour la compréhension de la relation structure-activité (par exemple pour le "drug-design), et l'étape de cristallisation des biomolécules est souvent limitante.
(à telecharger) Using Temperature To Crystallize Proteins: A Mini-Review
(à telecharger) New approaches on crystallization under electric fields
(à telecharger): Protein Crystallization: Contribution of Small-Angle X-ray Scattering (SAXS)
- Approches Classique
- Approches Non-Classique de la Cristallisation
- Les Milieux Confinés
- La microfluidique
- Interactions Moléculaires, Structuration, Assemblage et Cristallisation des Biomolécules
|
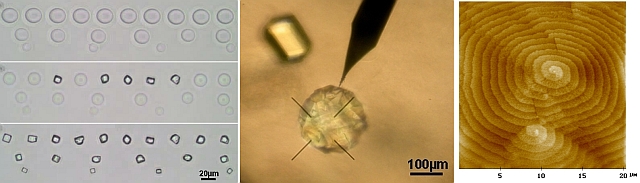
| Observation par microscopie de la cristallisation en milieu confiné: sursaturation élevée, nucléation et croissance ultra-rapide et 1 cristal par goutte. | Cristal de protéine (lysozyme) obtenu en presence d'un champ electrique localisé. | Observation par AFM (microscope à force atomique) en solution de la face (001) d'un cristal
de protéine (alpha-amylase) : on peut voir l'interaction de deux spirales de croissance éloignées
(hauteur des marches générées 50 Å).
contact : webmaster@cinam.univ-mrs.fr
|
