Nanosystèmes de dendrimères auto-assemblés pour l’imagerie par résonance magnétique au fluor spécifique et le traitement théranostique efficace des tumeurs
Proc. Natl. Acad. Sci. U.S.A. 2024, 121, e2322403121. DOI: 10.1073/pnas.2322403121.
Zhenbin LYU1,2,#, Brigino RALAHY1,#, Teodora-Adriana PERLES-BARBACARU3,#, Ling DING1,3,#, Yifan JIANG1, Baoping LIAN4, Tom ROUSSEL1, Xi LIU1,5, Christina GALANAKOU1, Erik LAURINI6, Aura TINTARU2, Suzanne GIORGIO1, Sabrina PRICL6,7, Xiaoxuan LIU4, Monique BERNARD3, Juan IOVANNA5, Angèle VIOLA3, Ling PENG1
L’imagerie par résonance magnétique du fluor (IRM-19F) est particulièrement prometteuse dans le domaine biomédical en raison de l’absence de fluor endogène dans la plupart des tissus biologiques. Mais, les applications de l’IRM-19F ont été limitées jusqu’à présent en raison du manque d’agents d’imagerie ayant une teneur élevée en fluor et des propriétés de relaxation adéquates pour l’IRM-19F, tout en étant non toxiques et solubles dans l’eau.
L’équipe de Ling Peng de laboratoire Centre Interdisciplinaire de Nanoscience Marseille (CINaM) a développé des agents d’imagerie innovants constitués de nanomicelles supramoléculaires auto-assemblés (1c@) formées à partir d’un dendrimère amphiphile fluoré 1c (Figure 1). L’incorporation de groupements chargés négativement aux extrémités des dendrimères, adjacents aux groupements fluorés, empêche l’agrégation intra et intermoléculaire par répulsion électrostatique et autorise en même temps une teneur élevée en fluor, favorisant la mobilité des groupements fluorés ainsi que la solubilité des dendrimères en milieu aqueux qui présentent des temps de relaxation favorables à l’IRM-19F (Figure 2). Un agent d’imagerie (DiR) pour la fluorescence proche infra-rouge (NIRF) ainsi qu’un agent anticancéreux, le paclitaxel (PTX), ont été encapsulés dans ces nanomicelles, permettant la détection des tumeurs par deux modalités d’imagerie, en vue d’une application théranostique dans un modèle de cancer (Figure 3).
En particulier, l’encapsulation de DiR ou du paclitaxel par le nanosystème supramoléculaire n’a pas altéré les propriétés de relaxation des noyaux 19F situés à la surface de la nanomicelle, ces agents étant suffisamment distants des noyaux fluor pour éviter toute interférence.
Dans cette étude, le DiR et le paclitaxel ont été utilisés comme agents pharmaceutiques modèles afin de démontrer l’efficacité de l’imagerie multimodale IRM-19F/NIRF et de la théranostique utilisant les agents dendrimères supramoléculaires auto-assemblés. Le dendrimère 1c@ a été évalué sur un modèle de tumeur pancréatique, un cancer pour lequel il n’existe pas de méthode de détection précoce adéquate ni de traitement efficace. Les études par IRM-19F réalisées au Centre de Résonance Magnétique Biologique et Médicale (CRMBM) et par imagerie NIRF chez les souris xénogreffées ont confirmé la capacité des deux modalités à imager spécifiquement les tumeurs et démontré l’efficacité de l‘agent théranostique pour le traitement des tumeurs, qui s’est révélé plus performant que le paclitaxel seul (Figure 3).
Ces nanonystèmes à base de dendrimères sont des agents prometteurs pour une prise en charge théranostique permettant la détection et le traitement simultanés de tumeurs. Cette étude montre aussi qu’il serait possible, en exploitant la chimie des dendrimères supramoléculaires auto-assemblés, de développer rapidement un large éventail d‘agents théranostiques basés sur l’IRM-19F qui pourraient être utilisés dans de futures applications en médecine personnalisée.
Fig. 1 Schematic illustration of self-assembling supramolecular dendrimer nanosystems for fluorine magnetic resonance imaging (19F-MRI), 19F-MRI-based multimodal imaging and theranostics. (A) Self-assembly of a fluorinated amphiphilic dendrimer into nanomicelles in the absence and/or presence of the NIRF probe DiR and the anticancer drug paclitaxel (PTX) within the supramolecular dendrimer core for 19F-MRI, bimodal 19F-MRI and NIRF imaging as well as 19F-MRI-based theranostics for cancer detection and treatment. (B) Chemical structures of the amphiphilic dendrimer 1c designed and studied for 19F-MRI.
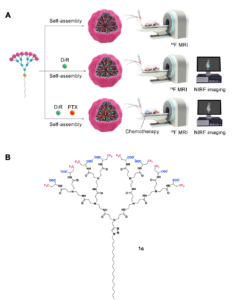
Fig. 2 Self-assembling of the amphiphilic dendrimer 1c into nanomicelles 1c@ for use as an imaging agent for fluorine magnetic resonance imaging (19F-MRI). (A) Dynamic light scattering results and (B) transmission electron microscopy image of the self-assembled 1c@ nanomicelles. (C) 19F-NMR spectrum of 1c@ in D2O. (D) 19F magnetic resonance relaxation time constants (T1 and T2) for 1c@ at a magnetic field strength of 7 T and 20°C. (E) In vitro 19F-MR images of 1c@ at four different concentrations. (F, G) In vivo 1H-MR anatomical images (top), 19F-MR images (middle), and overlay of 1H-MR and 19F-MR images (bottom) of tumors in pancreatic cancer xenograft mice 24 h after intravenous injection of 1c@ at 1c concentrations of (F) 0.208 mmol/kg and (G) 0.104 mmol/kg (corresponding to fluorine concentrations of 5.00 and 2.50 mmol/kg, respectively). MR images were acquired in the sagittal plane with respect to the mouse.
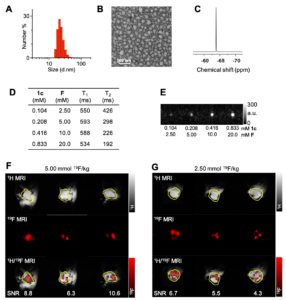
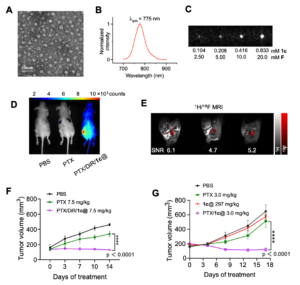
Fig. 3 The anticancer drug paclitaxel (PTX) and the near-infrared fluorescence (NIRF) dye DiR encapsulated within 1c@ for 19F-MRI-based multimodal imaging and theranostic treatment of tumor in pancreatic cancer xenograft mice. (A) Transmission electron microscopy image of PTX/DiR/1c@. (B) Normalized fluorescence emission spectrum of PTX/DiR/1c@. (C) In vitro 19F-MR images of PTX/DiR/1c@. (D) In vivo NIRF imaging of pancreatic cancer xenograft mice 48 h after injection of PTX/DiR/1c@. (E) 19F-MRI superimposed on anatomic 1H-MRI of tumors in pancreatic cancer xenograft mice 48 h after accomplished treatment with of PTX/DiR/1c@. MR images were acquired in the sagittal plane with respect to the mouse. (F, G) Tumor growth inhibition in tumor-xenograft mice following intravenous injection of (F) PTX/DiR/1c@ at a PTX concentration of 7.5 mg/kg or (G) PTX/1c@ at a PTX concentration of 3.0 mg/kg twice per week for 2 weeks. Statistical differences were assessed using two-way ANOVA with Tukey’s multiple comparison test.